临床与基础医学院(基础医学研究所)临床医学(卓越)专业2021级本科生乔欣羽同学在Cell Communication and Signaling(IF=8.4,中科院二区)以第一作者身份发表题为“Endothelial cell dynamics in sepsis-induced acute lung injury and acute respiratory distress syndrome: pathogenesis and therapeutic implications”的综述文章。该文系统梳理了脓毒症诱导急性肺损伤/急性呼吸窘迫综合征(ALI/ARDS)中内皮细胞的动态变化及其与免疫细胞、基质细胞的相互作用,并探讨了靶向内皮细胞的潜在治疗策略。
聚焦临床难题:脓毒症相关肺损伤的机制探索
脓毒症是临床常见的危重症,由感染引发的全身炎症反应综合征可导致多器官功能障碍,其中肺部是最易受累的器官。流行病学数据显示,脓毒症患者90天死亡率高达35.5%,而在巴西一项多中心研究中,ICU脓毒症患者死亡率甚至达到55.7%。脓毒症诱导的急性肺损伤(ALI)及其最严重形式急性呼吸窘迫综合征(ARDS),临床表现为难治性低氧血症、呼吸窘迫和非心源性肺水肿,是导致脓毒症患者死亡的重要因。
尽管临床现有治疗策略包括早期抗感染、血管活性药物支持等,能一定程度延长患者生存时间、降低短期死亡率,但针对ALI/ARDS根本发病机制的有效治疗药物仍然缺乏。柏林定义将ALI与ARDS统一纳入诊断标准,两者主要区别在于氧合指数:ALI为PaO2/FiO2 ≤300 mmHg,ARDS则≤200 mmHg。然而,从机制研究到临床转化的瓶颈,使得这一领域的治疗进展缓慢。
综述核心内容:内皮细胞——肺损伤的关键“守门人”
血管内皮由内皮细胞(ECs)构成,沿血管内壁形成单层屏障,在肺部病理生理过程中扮演多重角色。它既是血液与组织之间的半透性界面,也是调控炎症反应的重要参与者。近年来研究证实,内皮细胞功能障碍是脓毒症诱导ALI/ARDS的核心环节之一。
1. 内皮屏障破坏与血管通透性增加
过度炎症反应导致内皮细胞活化,引发糖萼降解、细胞间连接破坏,使得血管通透性增加。循环中的液体、大分子物质和白细胞得以进入肺泡,造成肺泡水肿和中性粒细胞浸润——这是ALI/ARDS患者死亡率升高的重要原因。
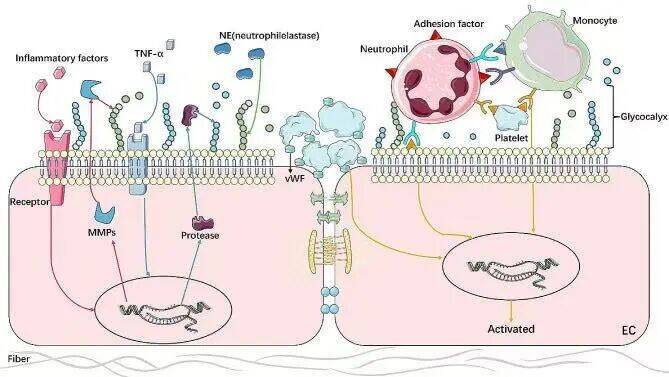
2. 内皮细胞与免疫细胞的“对话”
内皮细胞不仅是被动屏障,更主动参与免疫调节。活化的内皮细胞表达黏附分子,招募并激活中性粒细胞、巨噬细胞等免疫细胞,放大局部炎症反应。这种细胞间相互作用形成恶性循环,加剧肺组织损伤。
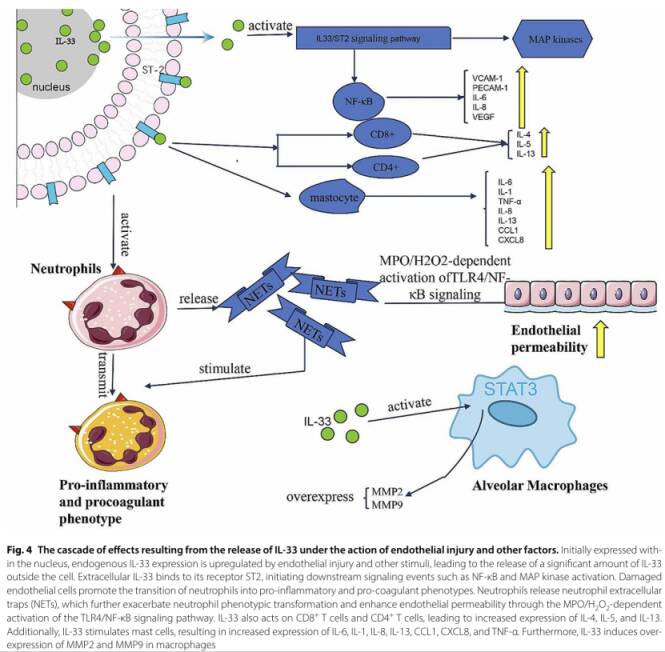
3. 内皮细胞与基质细胞的互作网络
综述特别强调了内皮细胞与肺上皮细胞、成纤维细胞等基质细胞的相互作用。这些细胞通过多种信号通路(如炎症通路、氧化应激通路等)相互影响,共同决定肺损伤的进展与修复方向。
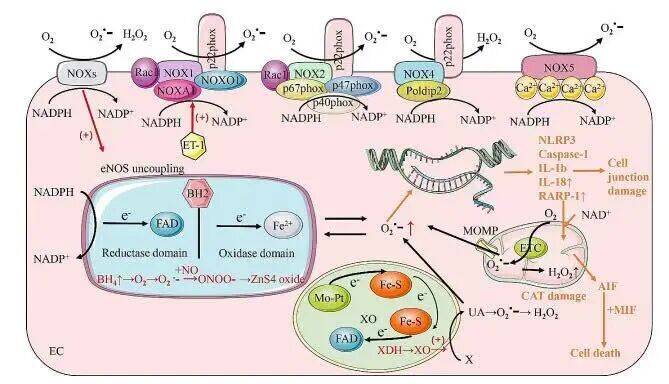
基于对内皮细胞功能的深入认识,综述进一步探讨了靶向内皮细胞的治疗前景:
· 直接保护内皮糖萼、稳定细胞间连接
· 调节内皮细胞与免疫细胞的相互作用,阻断炎症级联反应
· 干预关键信号通路,恢复内皮细胞正常功能
文章指出,未来需要聚焦细胞功能特征的机制性临床试验设计,同时发展能够评估临床内皮细胞功能的诊断方法,以实现对脓毒症患者内皮保护的精准干预。
谈及这篇综述的缘起,乔欣羽同学表示: “当时对脓毒症相关的器官损伤机制很感兴趣,查阅文献后发现内皮细胞在其中的作用非常关键,但国内相关的系统综述较少。” 写作过程历时近一年,累计阅读文献500余篇。“最难的是把不同研究领域的发现整合成一个有逻辑的故事——内皮细胞的屏障功能、免疫调节、与基质细胞的互作,这些线索需要串联起来。” 在丰秀静教授的指导下,最终完成了综述文章的撰写、修改和发表。
“作为本科生发表综述,最大的收获不是文章本身,而是学会了如何提出问题、如何构建论证、如何与文献‘对话’。”乔欣羽说,这段科研训练让他对未来的临床和研究道路有了更清晰的认识。
审核:邱建峰 谢建立 编辑:张晓宁 供稿:乔欣羽