2017年诺贝尔生理学或医学奖背后的昼夜节律分子机制
编者按
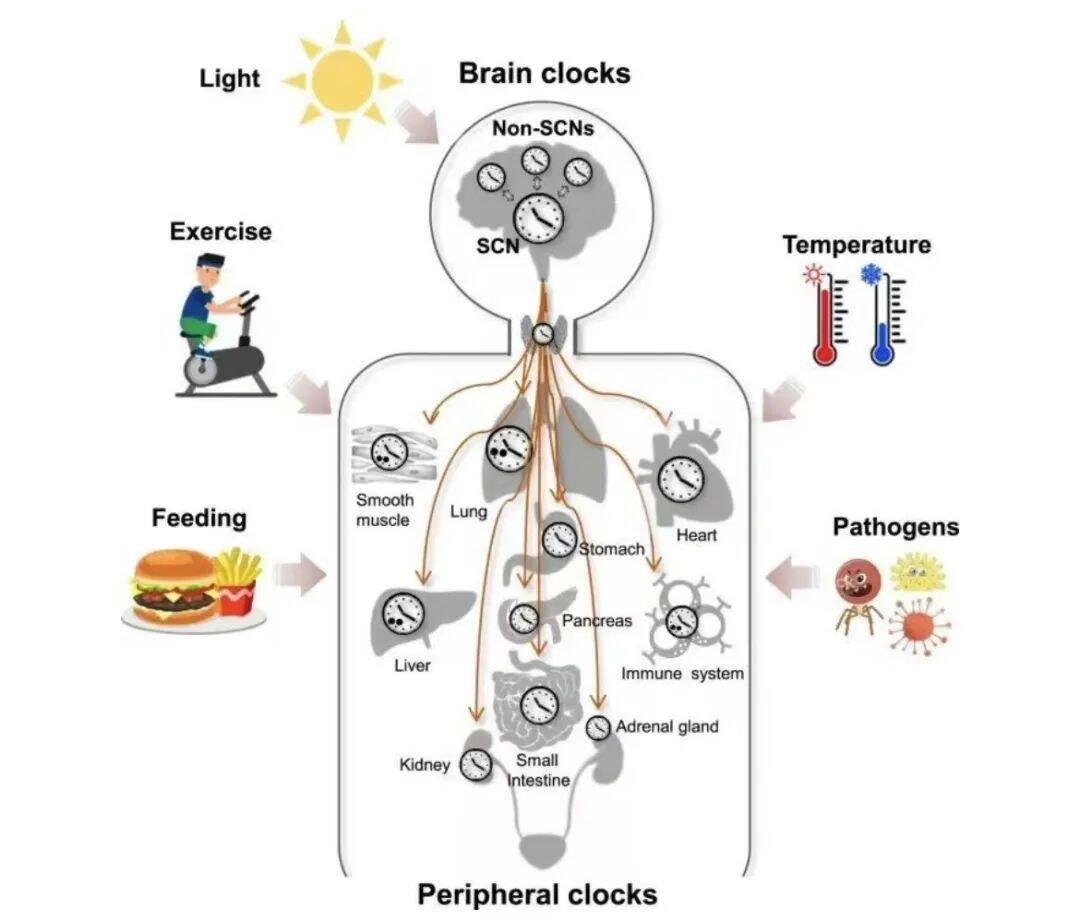
从果蝇到人类,生物体的生理活动与地球自转形成24小时周期紧密同步。熬夜的危害、倒时差的困扰,睡眠障碍与代谢疾病的关联,都与本期小医将介绍的2017年诺贝尔生理学或医学奖关于昼夜节律分子机制有密切关联,让我们一起探寻其中的奥秘。
探密诺奖:荣耀与意义
2017年诺贝尔生理学或医学奖授予了杰弗里·C·霍尔(Jeffrey C. Hall)、迈克尔·罗斯巴什(Michael Rosbash)和迈克尔·W·扬(Michael W. Young),以表彰他们发现了昼夜节律的分子机制。这一发现如同在生命科学的神秘花园中找到了一把关键的钥匙,为我们打开了理解生物内在时间调控机制的大门。昼夜节律是一种几乎存在于所有生命体中的内生计时系统,从微小的单细胞生物到复杂的人类,它在生物的睡眠 - 觉醒周期、新陈代谢、激素分泌等诸多生理过程中都起着至关重要的作用。然而,这一机制的揭秘之路并非坦途,三位科学家在探索过程中也遭遇了重重困难和质疑。

探索之旅:从现象到分子机制
早在20世纪70年代,科学家们就已经知道生物体内存在昼夜节律,但对于其背后的分子机制却一无所知。霍尔、罗斯巴什和扬选择了果蝇作为研究模型。他们对果蝇的日常行为节律产生了浓厚的兴趣,观察到果蝇的活动、休息有着非常规律的周期。通过大量的遗传学实验,他们发现了一个关键基因——period基因(简称per基因)。他们发现,per基因的表达水平呈现出昼夜周期性变化。进一步研究表明,per基因所编码的蛋白质PER会在夜间积累,在白天降解。然而,这一过程并非简单的线性关系。随着研究的深入,他们发现了一个复杂的反馈调节机制。
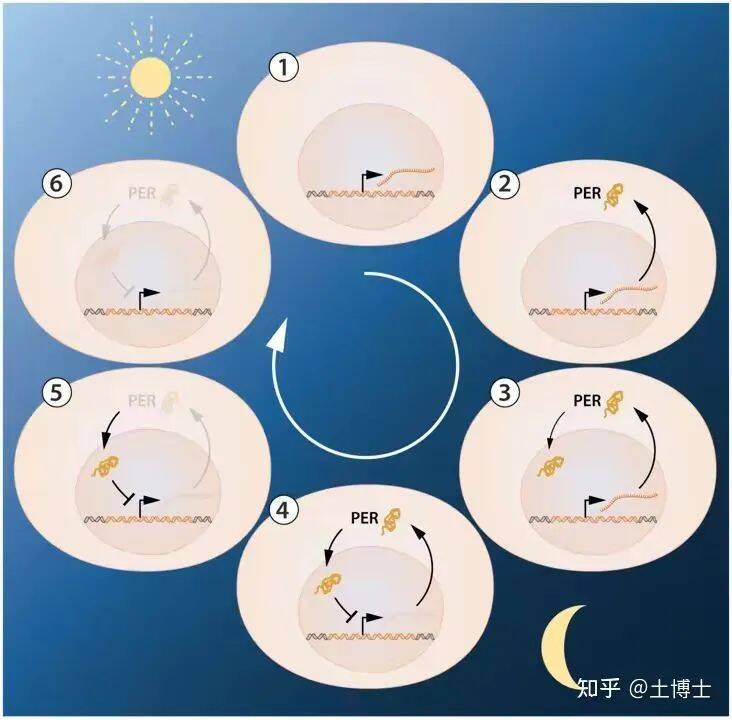
原来,PER蛋白会进入细胞核,反过来抑制自身基因(per基因)的转录。这就形成了一个负反馈回路:当per基因转录产生PER蛋白,PER蛋白积累到一定程度后,就会抑制per基因的进一步转录,从而使PER蛋白的水平下降;当PER蛋白水平降低到一定程度时,per基因又可以重新开始转录。
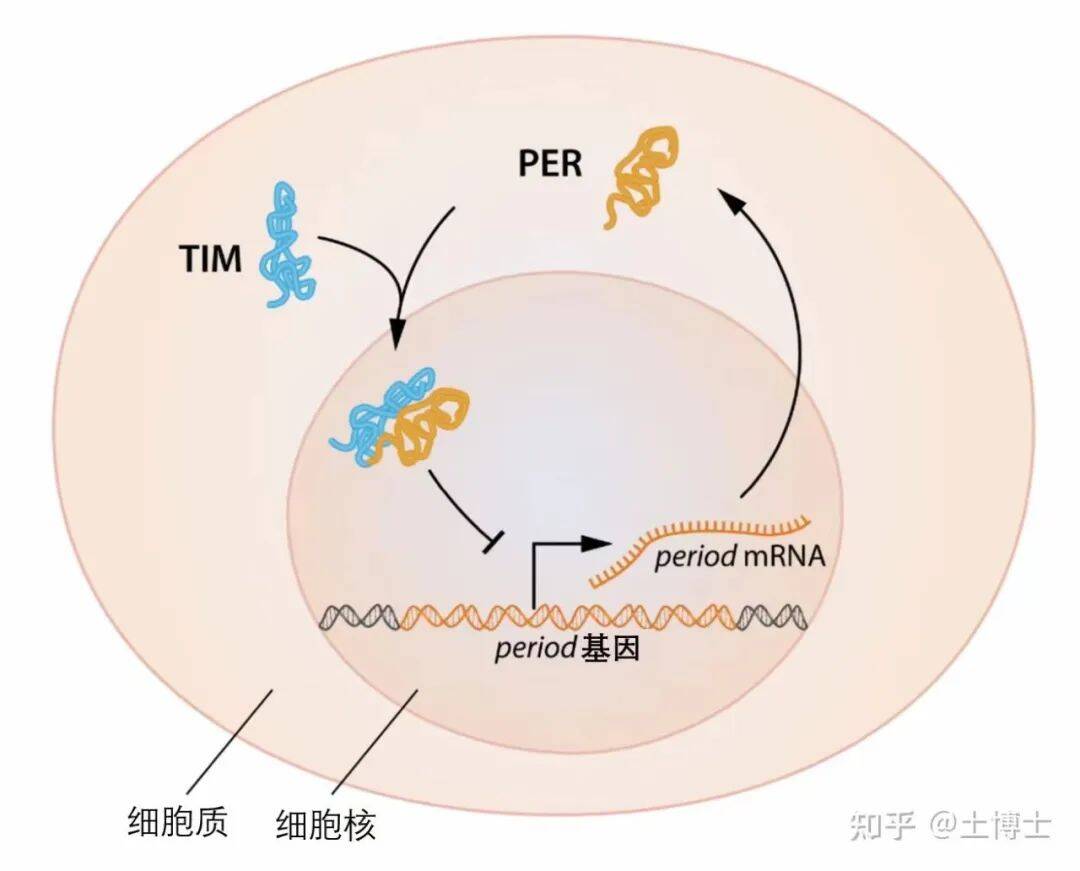
这种分子水平的昼夜节律调节机制的发现,于1984年在顶级学术期刊上发表。但这一成果在当时并未立即得到广泛认可。在后续的研究中,他们不断深入挖掘,发现了更多参与这一机制的基因和蛋白质,例如tim基因(timeless基因)及其编码的TIM蛋白等,它们与per基因和PER蛋白相互作用,共同维持着精确的昼夜节律。
探索精神:奉献与传承
霍尔、罗斯巴什和扬在昼夜节律研究中展现的坚持与专注,如黄钟大吕,振聋发聩,深刻启迪医学生。医学之路,恰似布满荆棘的险途,复杂知识如浩渺烟海,科研难题似巍峨雄峰。然他们于冷遇中坚守初心,在孤寂里砥砺奋进的历程,便是医学生前行的圭臬。当以其为范,怀精卫填海之信念,抱夸父逐日之勇毅,焚膏继晷,兀兀穷年,于医学知识的瀚海破浪,在科研困境的泥沼突围,方有希望冲破阴霾,为攻克疑难病症、推动医学进步铸不朽之勋,让生命之花因医学的光辉而绚烂绽放。
供稿:张立霖 张静蕾 燕昭彤 责任编辑:韩馨 审核:岳芸